Seit 2003 ernennt der Bundesverband Menschen für Tierrechte in Zusammenarbeit mit seinen Mitgliedsvereinen das „Versuchs- tier des Jahres“. Als „Schädling“ und Krankheitsüberträger stigmatisiert, wird der kleine Säuger zum Freiwild und wird fast manisch verfolgt, vergiftet und erschlagen. Auch die Ratte im Labor und als „Futtertier“ im Zoogeschäft, beides Abkömmlinge der Wanderratte, erwartet meist kein besseres Schicksal. Die Ratte ist für die Forschung ein Versuchstier, über das sich wenige empören.
Geringere Leidensfähigkeit nicht erwiesen
 Ratten werden in der Tierversuchssystematik niedriger bewertet. Es wird ihnen unterstellt, dass sie weniger leiden als z.B. ein Affe. Aber die Hintergründe für ihren häufigeren Einsatz sind praktischer und wirtschaftlicher Natur. Sie werden bevorzugt in Giftigkeitstests eingesetzt, weil einmal verabreichte Substanzen sicher im Magen bleiben – die Ratte kann im Gegensatz zu anderen Tieren nicht erbrechen. Behörden begründen die Verwendung von Ratten einfach auch mit vorhandenen umfangreichen Daten zu ihrer Physiologie und Pathologie, ihrer relativ kurzen Lebensspanne und der zuchtbedingten leichten Ausbildung von Tumoren. Gemeinsam mit unserem Schirmherrn Prof. emer. Franz Gruber macht der Verband das Leid der Ratten im Labor öffentlich und macht Druck für die Entwicklung tierversuchsfreier Verfahren – damit die qualvollen Tierversuche endlich beendet werden.
Ratten werden in der Tierversuchssystematik niedriger bewertet. Es wird ihnen unterstellt, dass sie weniger leiden als z.B. ein Affe. Aber die Hintergründe für ihren häufigeren Einsatz sind praktischer und wirtschaftlicher Natur. Sie werden bevorzugt in Giftigkeitstests eingesetzt, weil einmal verabreichte Substanzen sicher im Magen bleiben – die Ratte kann im Gegensatz zu anderen Tieren nicht erbrechen. Behörden begründen die Verwendung von Ratten einfach auch mit vorhandenen umfangreichen Daten zu ihrer Physiologie und Pathologie, ihrer relativ kurzen Lebensspanne und der zuchtbedingten leichten Ausbildung von Tumoren. Gemeinsam mit unserem Schirmherrn Prof. emer. Franz Gruber macht der Verband das Leid der Ratten im Labor öffentlich und macht Druck für die Entwicklung tierversuchsfreier Verfahren – damit die qualvollen Tierversuche endlich beendet werden.
 Mehr als 320.000 Ratten im Tierversuch
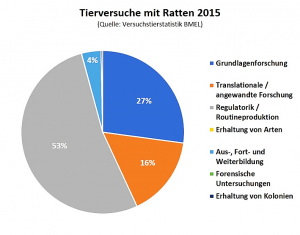
Mehr als 320.000 Ratten im Tierversuch
In 2015 wurden 36.297 weniger Ratten tierexperimentell genutzt als 2014 (16). Insgesamt wurden 320.629 Ratten eingesetzt. Davon wurden 5.604 Ratten (1,8 Prozent) zwei- oder mehrfach verwendet (17). Es gab einen Rückgang von 12,96 auf 11,65 Prozent aller Tierversuche. Damit steht die Ratte noch immer an zweiter Stelle in der Statistik.
Bestimmte Zuchtformen für bestimmte Forschungsgebiete
Das Wistar Institute for Anatomy and Biology der University of Pennsylvania, Philadelphia begann etwa 1906, Ratten als „standardisierte“ Labortiere zu züchten. Die Tiere nennt man „Wistar-Ratten“, es sind Albinoratten, die eine geringe Häufigkeit von Spontankrebs-erkrankungen besitzen. Sie werden heute in vielen Forschungslaboren auf der ganzen Welt eingesetzt. Von den „Wistar-Ratten“ wurde eine andere Laborzuchtform weitergezüchtet, die „Sprague-Dawley“-Ratte: es ist ein Albino-Rattenstamm, der als Versuchstier wegen seiner Gutmütigkeit und leichten Handhabung häufig im Bereich der Toxikologie, Pharmakologie, sowie in der Reproduktions- und Verhaltens-Forschung eingesetzt wird.
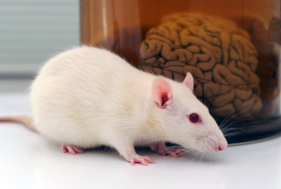
Auf dem Gebiet der Alters- und Krebs-Forschung werden dagegen sogenannte „Fischer-344-Ratten“ eingesetzt. Durch Inzucht sind diese Albinos alle genetisch identisch. Des Weiteren gibt es die „Lewis-Ratten“. Sie besitzen eine genetische Disposition für entzündliche Erkrankungen. Sie werden daher gerne zu Studien über Autoimmunerkrankungen eingesetzt. Spezielle auf Krankheit gezüchtete „Tiermodelle“ sind die „BB-Ratte“ mit der Ausprägung des Diabetes Typ 1 und die „SHR-Ratte“ mit Bluthochdruck-Beschwerden.
Zahl der gentechnischen Manipulationen steigt an
Noch ist die Maus das am häufigsten gentechnisch manipulierte Tier, doch auch die Zahl der „Gentech-Rattenmodelle“ wächst. In 2015 wurden 12.806 Ratten gentechnisch verändert. Gegenüber dem langjährigen Mittel (7067, für 2014 lagen keine Daten vor) ist der Anteil an gentechnisch veränderten Ratten um 80 Prozent gestiegen. Es werden Nacktratten für die Krebsforschung erzeugt, deren Immunsystem ausgeschaltet wurde. Es gibt Ratten mit künstlich erzeugtem Diabetes, mit Nierenerkrankungen, Herzinsuffizienz, Bluthochdruck, 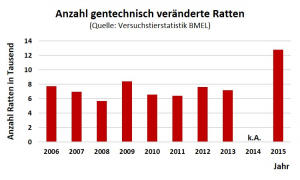 Darmkrebs oder Chorea Huntington.
Darmkrebs oder Chorea Huntington.
Gentechnisch veränderte Ratten
Für die Forschung wurden und werden Ratten genetisch verändert, um definierte Krankheiten oder krankhafte Veränderungen an Körper oder auch Psyche in den Tieren zu entwickeln. Solche Ratten werden als „Krankheitsmodelle“ bezeichnet und durch Weiterselektion natürlicher Mutationen oder durch gentechnische Manipulationen erzeugt. Hierbei kann es möglich sein, dass ein Gen ausgeschaltet, aktiviert oder ein zusätzliches Gen, z.B. vom Menschen eingebracht wird. Solche Tiere werden als „transgene“ Tiere bezeichnet.

„Überproduktion“ wird nicht erfasst
In der Regel werden nur die „gängigen“ lebend bereitgehalten. Die anderen Linien werden als tiefgefrorene Embryonen oder befruchtete Eizelle bevorratet. Erst bei Eingang einer Kundenbestellung werden sie aufgetaut und weiblichen Ratten in die Gebärmutter eingepflanzt. Am Ende der Trächtigkeit wird den keimfrei gehaltenen weiblichen Ratten die Gebärmutter entnommen, um daraus unter sterilen Bedingungen die Rattenjungen zu gewinnen, welche wiederum von keimfreien Ammenmüttern gesäugt werden. Vom Hersteller nicht ausgelieferte, „fehl“‐ oder „überproduzierte“ Tiere, Muttertiere nach Kaiserschnitt sowie solche Tiere, die unplanmäßig Kontakt zu ggfs. unsterilen Bereichen hatten und somit als nicht mehr keimfrei gelten, werden getötet. Wie viele Tiere dies betrifft, wird nirgends erfasst.
Beispiele für Tierversuche mit Ratten
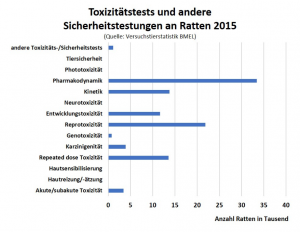 In den gesetzlich vorgeschriebenen Tests ist die Ratte das klassische Tier für Giftigkeits- und Sicherheitstests von Chemikalien, Arzneimitteln, Bioziden und Pestiziden. Dabei spielen vor allem Test auf Pharmakodynamik (Wechselwirkung mit Zellrezeptoren und Wirkung im Körper), Verstoffwechslung, Langzeittests und Tests auf Reproduktionsfähigkeit und Entwicklung der Nachkommen eine große Rolle.
In den gesetzlich vorgeschriebenen Tests ist die Ratte das klassische Tier für Giftigkeits- und Sicherheitstests von Chemikalien, Arzneimitteln, Bioziden und Pestiziden. Dabei spielen vor allem Test auf Pharmakodynamik (Wechselwirkung mit Zellrezeptoren und Wirkung im Körper), Verstoffwechslung, Langzeittests und Tests auf Reproduktionsfähigkeit und Entwicklung der Nachkommen eine große Rolle.
Toxizitätstest und Sichereitsprüfungen
Unbeweglich Gift atmen
Z.B. müssen Ratten im Rahmen von Langzeittests 90 Tage lang 5 Tage in der Woche je 6 Stunden Pigmentstaub aus Titandioxid einatmen. Dafür werden die in eine Apparatur eingequetscht, in der sie sich nicht bewegen können. Danach werden sie getötet und das Gewebe untersucht.

Ratten in Reproduktions- und Entwicklungs-Giftigkeitstests
Ratten müssen häufig in Reproduktions- und entwicklungstoxikologischen Tests leiden. Bei diesen Tests soll untersucht werden, ob sich ein Stoff schädlich auf die Reproduktionsfähigkeit und die Entwicklung der Organe oder des Nervensystems der Nachkommen auswirkt. Dazu wird Rattenmüttern eine Testsubstanz in mindestens drei unterschiedlichen Dosierungen während der Trag- und Laktationszeit verabreicht. Dies erfolgt erzwungen über eine Schlundsonde, über das Trinkwasser, per Inhalation oder über die Haut. Danach werden die Mütter getötet und eine bestimmte Anzahl der Nachkommen, die anderen werden weiterverpaart und ihre Reproduktionsfähigkeit anhand ihrer Organe und ihrem Verhalten untersucht. Andere Welpen werden unter anderem funktionellen Untersuchungen und Verhaltenstests unterzogen.
Dabei werden auch motorische, sensorische Funktionen sowie Lernen und Erinnern überprüft. Um den Orientierungssinn zu testen, wird auch der berüchtigte Water-Maze-Test eingesetzt. Dabei muss die Ratte eine unter der Wasseroberfläche befindliche, nicht sichtbare Plattform finden und sich deren räumliche Position merken. Einige Testrichtlinien verlangen, neben der Elterngeneration zwei weitere Generationen (also Kinder- und Enkel) zu untersuchen. So müssen je nach Testrichtlinie bis zu 2600 Tiere pro Substanz sterben. Um die hohe Zahl der Tiere zu reduzieren, haben die Regulationsbehörden die sogenannte die „Extended-One-Generation-Studie“ eingeführt. Mit ihr kann die Zahl der Tiere um 1000 pro Substanz reduziert werden.

Parkinson-Rattenmodell
Zur Behandlung der Parkinson-Erkrankung werden heutzutage Dopamin produzierende Zellen in Patienten implantiert. Dies ist jedoch nicht nebenwirkungsfrei. Um eine neue, nebenwirkungs-freie Methode zu testen, wurde in Ratten zunächst ein parkinsonähnlicher Zustand ausgelöst, indem Dopamin produzierende Nervenzellen durch Injektion eines Giftstoffes in einer Hirnhälfte abgetötet wurden. Die Tiere entwickelten dadurch einseitig Symptome einer Parkinsonkrankheit. In einer zweiten Operation wurden neue Dopamin produzierende Zellen implantiert. Nach einer bestimmten Untersuchungszeit wurden die Tiere getötet.
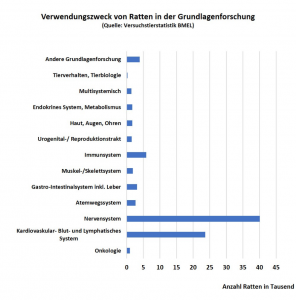 Ratten in der Grundlagenforschung
Ratten in der Grundlagenforschung
Ratten in der Alkohol- und Suchtforschung
Um herauszubekommen, inwieweit das „Kuschelhormon“ Oxytocin einen positiven Einfluss auf das Verlangen nach Alkohol hat, wurden Ratten künstlich alkoholabhängig gemacht. Dann wurde in den Rattengehirnen der Oxytocin-Rezeptor mit einer chemischen Substanz blockiert. Anschließend wurde das „Kuschelhormon“ Oxytocin in die Bauchhöhle gespritzt, um die Auswirkungen des Hormons auf das Suchtverhalten zu untersuchen. Die Tiere litten dabei mehrfach: Einmal unter den Eingriffen, dann unter den Untersuchungen und den Entzugserscheinungen. Am Ende des Versuches steht – wie bei fast allen Versuchen – der Tod.
Äußerst Schmerzhaft: Osteoarthrosemodell Ratte
Ein sogenanntes Osteoarthrose-Modell zur Untersuchung von Gelenkproblemen kann über mehrere verschiedene Techniken im Tier erzeugt werden und führt immer zu schweren Leiden und Schäden. In einem Fall wird Monoiodoacetat ins Kniegelenk gespritzt, wodurch schnell eine Schmerz-Reaktion im Kniegelenk ausgelöst wird. Die Schmerzstärke wird durch die Höhe der Dosis bestimmt. Eine Injektion der Substanz in die Gelenkhöhle unterbricht die Glykolyse der knorpelbildenden Zellen und zum Ausfall eines bestimmten Enzyms, was zum Absterben der knorpelbildenden Zellen, zum Zusammenbruch des darunterliegenden Knochens und zu schmerzhaften Entzündungsprozessen führt. Mit dem so erzeugten Rattenmodell werden Medikamente getestet, mit dem Ziel, die Entzündung zu beseitigen oder zumindest zu lindern. Häufig wird die Dosis oder das Verfahren so gewählt, dass „nur“ die Entzündung, und kein Zusammenbruch im Kniegelenk erzeugt wird. Die Tiere verlagern ihr Schwergewicht auf die gesunde Seite und vermeiden nach Möglichkeit, sich viel zu bewegen. Am Ende werden die Tiere getötet. Trotz der vielen Modelle, die mit Tierleid verbunden sind, ist kein Medikament entwickelt oder zugelassen worden, das den Krankheitsverlauf der Osteoarthrose nachweislich verbessert.
Ersatzverfahren für Rattenversuche
Initiative für einen Wegfall der akuten Toxizitätstests
Die meisten Chemikalien, die in Europa produziert werden, sind von geringer Toxizität. Sie werden bisher in rechtlich vorgeschriebenen akuten Toxizitätstests, in 28-Tage-Tests und ab einer bestimmten jährlichen Produktionsmenge auch in 90-Tage-Tests in Nagetieren (Ratte und Maus) geprüft. Jetzt haben Wissenschaftler erfreulicherweise vorgeschlagen, auf die akuten Toxizitätstests zu verzichten. Denn die Daten aus 28-Tage-Studien erhalten alle notwendigen Informationen für eine Risikobewertung. Die Wissenschaftler sind überzeugt, dass für Substanzen von geringer Toxizität der 28-Tage-Test reichen kann, wenn Informationen aus verschiedenen zusätzlichen Quellen (in vitro-Tests, QSAR-Analysen und physikalisch-chemische Informationen) zusätzlich herangezogen werden.
Verzicht auf Tests des sogenannten „Six-Pack“
Aus den USA und Canada kam der Vorschlag, auf Tierversuche im Bereich der akuten Toxikologie komplett zu verzichten und sie ggfs. mit tierversuchsfreien Methoden durchführen zu lassen. Hierbei handelt es sich um Versuche aus dem sogenannten 6-Pack: Inhalationstoxikologie, orale Toxikologie, Hautätzung, Hautreizung, Hautsensibilisierung und Augenätzung. Die OECD hat hierzu bereits ein Dokument zur Verfahrensweise vorgelegt. Das neue Prinzip ist für Pestizide anwendbar und kann auch auf andere Chemikalien, auf Formulierungen und biologische Materialien übertragen werden.
Ersatzverfahren für in-vivo-Langzeittoxizität
Derzeit gibt es keine anerkannten Ersatzverfahren zum Tierversuch für regulatorische Zwecke im Bereich der Langzeittoxizität. Zahlreiche in-vitro-Verfahren wurden bereits entwickelt. An Modellverbesserungen wird gearbeitet. Bei der Entwicklung geeigneter tierfreier Testmethoden ist es nötig, die komplexen Vorgänge und Wechselwirkungen im Körper nachbilden zu können. Zwar wurden schon zahlreiche in-vitro-Verfahren entwickelt. Doch nach Ansicht der Europäischen Chemikalienagentur (ECHA) reichen sie nicht aus, um umfassende Aussagen zur Wirkung der Substanzen beispielsweise bei der Verstoffwechselung zu machen. Vorhersagen zu Aufnahme, Verteilung, Um- und Abbau sowie Ausscheidung von Substanzen können jedoch in Ansätzen mit einer Kombination aus mathematischen Modellen heute schon gemacht werden.
Verfahren in der Reproduktions- und Entwicklungstoxikologie

Das europäische Förderprojekt „EU ToxRisk“ befasst sich genau mit den noch fehlenden Verfahren, um den Tierversuch bei diesen gesetzlich vorgeschriebenen Tests abzulösen. Im Rahmen des Projekts werden Machbarkeitsstudien durchgeführt und Umsetzungsmöglichkeiten jenseits des Tierversuchs erarbeitet. Es werden u.a. Multi-Organ-Systeme im Miniaturformat eingesetzt. Zwar lassen sich mit der Chiptechnologie die Auswirkungen auf die Nachkommen nicht direkt simulieren. Zukünftig soll es aber möglich sein, die Auswirkungen der Substanzen auf die Fortpflanzungsorgane und die Organentwicklung per Chiptechnologie zu ermitteln.
Zukunft: Der Mensch auf dem Chip
Ein Lösungsansatz ist der 10-Organ-Chip, der auch das Hormon- und Immunsystem nachbilden wird. Eine Validierungsstudie des Berliner Unternehmens TissUse soll schon 2018 beginnen. Diese Organsysteme wären dazu geeignet, die noch bestehenden Lücken der vorhandenen Verfahren in Langzeitgiftigkeitstests zu schließen. Gleichzeitig wird an der Verbesserung der Leistungsfähigkeit bereits entwickelter Miniorgane (Organoide) gearbeitet.
Gegenwartsmusik: Humane Krankheitsmodelle statt genmanipulierte Ratten
Anstelle von Tiermodellen können heute humane Krankheitsmodelle in der Petrischale oder auf dem Chip erzeugt werden. Das ist bereits Gegenwartsmusik. Wie bei den gentechnischen Veränderungen beim Tier kann dafür ebenfalls die CrispR/Cas9-Methode genutzt werden. Das wichtigste Ziel von in-vitro-Krankheitsmodellen ist, die die mechanistischen Abläufe der Erkrankungen aufzudecken, um neue oder verbesserte Therapien zu entwickeln. Es gibt mittlerweile unzählige Krankheitsmodelle in der Petrischale für die Organe Herz, Lunge, Darm, Leber und Nieren. Weitere Modelle eignen sich für die Untersuchung der Blutbildung, der Gefäße, des Hormonhaushaltes, des Skeletts und des Nervensystems. Hinzu kommen Knorpelerkrankungsmodelle, Modelle der verschiedensten Infektions- und Krebserkrankungen sowie Schizophrenie-Modelle mit verschiedenen Gehirnregionen auf dem Chip.
Krankheitsmodell: Rauchmaschine mit Lung-on-a-Chip-Modell gekoppelt
In-vivo-Tierversuche an Ratten sind zum Testen inhalierbarer Substanzen ungeeignet, weil die Tiere durch den Mund atmen und abweichende fremdstoffmetabolierende Enzyme besitzen. Daher haben Forscher des Wyss Institute for Biologically Inspired Engineering an der Harvard-Universität in Boston zur Untersuchung der Auswirkungen des Rauchens z.B. eine kleine „Mikrolunge auf dem Chip“ mit menschlichen Bronchialepithelzellen mit einer Zigarettenrauchmaschine kombiniert und zu einem Mikrorespirator weiterentwickelt. Damit lassen sich z.B. negative Effekte des Rauchens, aber auch anderer inhalierbarer Substanzen auf die Lunge genauer untersuchen. Herkömmliche Zellkulturen sind durch ihre Statik dafür nicht geeignet. Es lassen sich lediglich Gase und Partikel auf die Oberfläche aufbringen und deren Auswirkungen auf die Zellen studieren. Tiefe Atemzüge sind jedoch nicht simulierbar.
Aber auch Lungenkrankheitsmodelle für die translationale Forschung gibt es bereits: Forscher der Universität Bern z.B. haben Lungenkrankheits-Modelle auf dem Chip entwickelt. Damit erforschen sie die Erkrankungen und testen Medikamente zur Behandlung dieser Erkrankungen. Die Forschergruppe hat bereits Lungenmodelle, Lungenmikrogefäßmodelle, Lungentumor- und Lungenfibrose-Modelle auf dem Chip entwickelt. Gerade Medikamente gegen Lungenfibrose haben mit herkömmlichen Testmethoden am Tier keine befriedigende Wirkung für die Patienten ergeben.
Chipmodelle auch zur Erforschung neuronaler und Sucht-Erkrankungen
Wissenschaftler der Harvard University haben ein multiregionales Brain-on-a-Chip-Modell entwickelt, das die Verbindungen zwischen drei verschiedenen Regionen des Gehirns modelliert. Die Forscher wollen damit untersuchen, wie sich Erkrankungen wie z. B. Schizophrenie auf die verschiedenen Gehirnregionen auswirken. Die Hirnregionen Amygdala, Hippocampus, präfrontaler Kortex sowie deren Nervenzellverbindungen wurden bereits auf einem Mikrochip konstruiert. Hauptangriffspunkt bei Schizophrenie sind die Nervenverbindungsstrukturen zwischen den einzelnen Hirnregionen. Das Modell ist geeignet, verschiedene Erkrankungen wie Drogenabhängigkeit, posttraumatische Belastungsstörungen und traumatische Hirnverletzungen zu untersuchen.
Ausblick: Nötig sind Investitionen und Kombinationsverfahren
Bei Ratte, Maus und Fisch wird der kontinuierliche Anstieg der Tierzahlen im Bereich der gentechnischen Veränderung besonders deutlich. Dies zeigt die Dringlichkeit eines Verbotes von Patenten auf Tiere sowie den Schutz der genetischen Integrität von Lebewesen. Dabei bieten humane Krankheitsmodelle ein großes Potential, um Krankheiten des Menschen zu untersuchen. Die Zukunft in der Grundlagenforschung muss deswegen heißen: Menschliche Krankheitsmodelle statt genmanipulierte Tiere.
Unabdingbar: Mehr Forschungsförderung
Um die Entwicklung neuer Verfahren sowie den Ausbau und die Kombination bereits vorhandener tierversuchsfreier Methoden zu beschleunigen, ist erhebliche Forschungsarbeit nötig. Deshalb muss deutlich mehr Forschungsförderung in die Entwicklung dieser Verfahren fließen. Darüber hinaus ist die Etablierung weiterer Lehrstühle für tierversuchsfreie Methoden, ein Ausbau der Förderung von Nachwuchswissenschaftlern, die finanzielle Absicherung potenzieller Methoden bis zu ihrer Anerkennung sowie schnelle Anerkennungsverfahren auf europäischer und internationaler Ebene notwendig. Denn die behördlichen Anerkennungsverfahren dauern mit 6 bis 15 Jahren immer noch viel zu lang. Weitere zielführende Maßnahmen für einen Paradigmenwechsel hin zu einer tierversuchsfreien Zukunft hat der Bundesverband in einem umfangreichen Maßnahmenkatalog zusammengestellt.
 Weitere ausführliche Informationen zum Versuchstier des Jahres 2017 lesen Sie in PDF-Format (31 Seiten), die wir Ihnen zum Herunterladen anbieten.
Weitere ausführliche Informationen zum Versuchstier des Jahres 2017 lesen Sie in PDF-Format (31 Seiten), die wir Ihnen zum Herunterladen anbieten.

Der Bundesverband dankt Prof. Dr. Franz Gruber für die Übernahme der Schirmherrschaft. Lesen Sie hier sein Grußwort.

